近日,我校龔其海教授團(tuán)隊(duì)在國(guó)際頂級(jí)期刊《Biomaterials》(IF: 12.8,中科院醫(yī)學(xué)1區(qū))在線發(fā)表了題為“α-Synuclein Targeted Therapy with Multiple Pathological Improvement for Parkinson’s Disease by Macrocyclic Amphiphile Nanomedicine”的高水平研究論文。論文第一作者為高健美教授,通訊作者為龔其海教授,共同第一作者為南開大學(xué)李文博博士,共同通訊作者為南開大學(xué)郭東升教授,我校為第一完成單位。
帕金森病(PD)是僅次于阿爾茨海默病的第二常見的神經(jīng)退行性疾病,致殘率和死亡率較高,嚴(yán)重影響患者生活質(zhì)量。現(xiàn)有傳統(tǒng)藥物僅能緩解PD癥狀,不能延緩其進(jìn)展,且存在不良反應(yīng)多等問題。因此,迫切需要研發(fā)更安全、有效治療PD的藥物。PD的主要病理特征是黑質(zhì)中多巴胺能神經(jīng)元缺失以及α-突觸核蛋白(α-syn)在神經(jīng)元細(xì)胞中呈纖維狀聚集。α-syn聚集體可損害神經(jīng)細(xì)胞的正常生理功能,是PD病理進(jìn)程中的關(guān)鍵因素。因此,尋求有效抑制α-syn聚集的策略或藥物對(duì)PD的防治具有重要的現(xiàn)實(shí)意義。
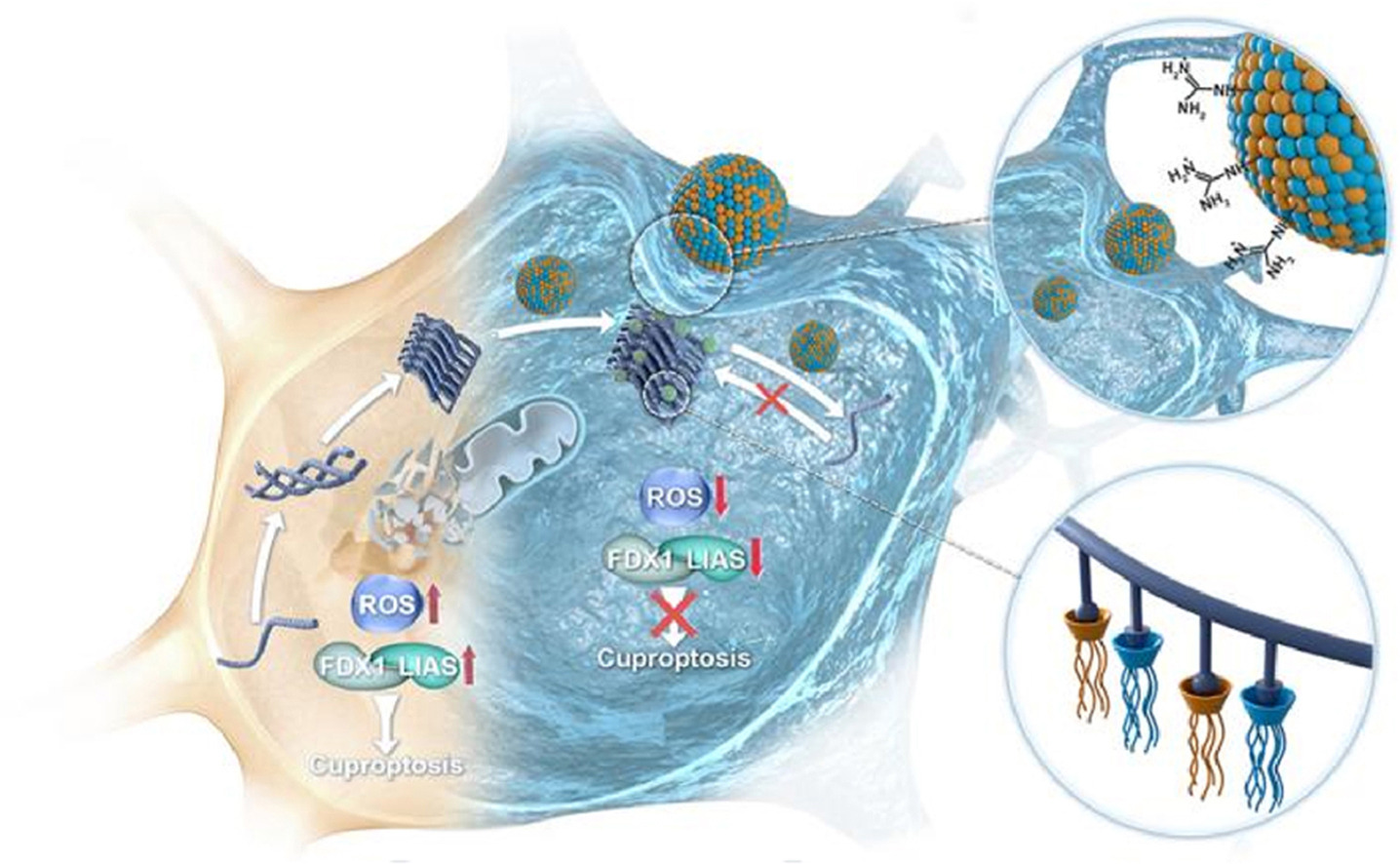
該研究通過藥學(xué)、材料與生物醫(yī)學(xué)的深度交叉,開發(fā)了一種基于杯芳烴與環(huán)糊精的大環(huán)兩親共組裝納米藥物(GCA-CD)。GCA-CD能夠選擇性的與α-syn結(jié)合,兼具高效分解α-syn聚集體和強(qiáng)大的跨膜能力,進(jìn)而發(fā)揮靶向抑制α-syn纖維化的作用。團(tuán)隊(duì)綜合運(yùn)用分子識(shí)別、體內(nèi)動(dòng)物實(shí)驗(yàn)、轉(zhuǎn)錄組學(xué)等技術(shù),揭示了GCA-CD通過抑制α-Syn纖維化發(fā)揮治療PD的作用,其機(jī)制可能與修復(fù)線粒體功能及調(diào)控銅死亡信號(hào)途徑有關(guān)。研究團(tuán)隊(duì)這一成果不僅為闡釋帕金森病的病理機(jī)制提供了新見解,也為基于大環(huán)超分子體系的神經(jīng)退行性疾病治療材料設(shè)計(jì)開辟了新方向不僅體現(xiàn)了藥學(xué)與材料科學(xué)交叉融合的創(chuàng)新優(yōu)勢(shì),也為未來開發(fā)兼具高效性與安全性的神經(jīng)疾病治療藥物奠定了重要基礎(chǔ)。
該研究獲得國(guó)家自然科學(xué)基金、貴州省高層次創(chuàng)新型人才“百層次”人才等項(xiàng)目的資助。(審核:一審李曉,二審上官騰飛,三審楊清玉、李均;圖文:高健美)
論文鏈接:https://doi.org/10.1016/j.biomaterials.2025.123378


